AG Gerold | Zelluläre Virologie
Ziel unserer Forschungsgruppe ist es, die zugrunde liegenden biochemischen Prinzipien einer Infektion von Wirtszellen durch Viren zu verstehen. Der Schwerpunkt unserer Studien liegt auf der Untersuchung des viralen Eintritts und der Replikation in Wirtszellen. Wir untersuchen Proteininteraktionen während des Lebenszyklus von Viren mit Hilfe von hochauflösender quantitativer Proteinanalyse. In den letzten Jahren haben wir Proteininteraktionen während der Infektion mit dem chronischen Hepatitis-C-Virus (HCV) und neu auftretenden, durch Insekten übertragenen Viren charakterisiert. Diese Studien wurden auch auf SARS-CoV-2 und RSV ausgedehnt. Langfristig kann das Wissen über Wirtsfaktoren für die Entwicklung von Antiinfektiva genutzt werden und zum Verständnis des Gewebe- und Wirtstropismus von Viren beitragen.
Das Auftreten von Viren ist eine globale Herausforderung, die durch anthropogene Veränderungen der Ökosysteme beschleunigt wird. So konnten sich virusübertragende Stechmückenarten infolge des Klimawandels nach Europa ausbreiten. Anhand von durch Mücken übertragenen Viren wie dem Chikungunya-Virus und respiratorischen Viren wie SARS-CoV-2 und RSV konzentrieren wir uns auf Proteinnetzwerke, die an der viralen Infektion beteiligt sind. Zu diesem Zweck setzen wir Techniken der Proteomik ein. Unsere Arbeit zielt darauf ab, Ähnlichkeiten und Unterschiede in der Nutzung von Wirtsfaktoren bei zoonotischen Viren zu ermitteln, d. h. Viren, die zwischen Tieren und Menschen übertragen werden. Dies wird neue Wege für die Entwicklung antiviraler Medikamente und das Verständnis des Wirts- und Gewebetropismus eröffnen, was letztlich zur Risikobewertung der Übertragungswege, des Krankheitsverlaufs und des Pandemiepotenzials von Viren beitragen wird.
Unsere Gruppe ist daran interessiert, die Protein- und Lipiddeterminanten von Virusinfektionen zu verstehen. Die Abbildung rechts zeigt ein Modell des Chikungunya-Virus-Replikationskomplexes an der Plasmamembran mit dem viralen Genom in der Mitte und den von uns identifizierten Wirtsproteinen und Lipiden, die in die Membran eingebettet sind. Der dodekamere Ring am Hals stellt das nicht-strukturelle Protein 1 (nsP1) des Chikungunya-Virus dar. Einzelheiten sind zu finden in Lasswitz et al., mBio 2022.
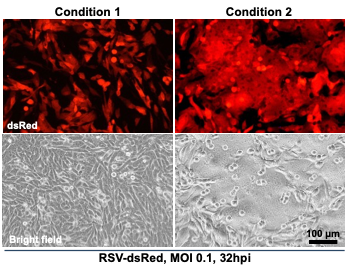
Abb. 1 Infektion von HEp-2-Zellen (menschliche Kehlkopfkrebszellen) mit RSV-dsRed (RSV-Stamm A2, der das rot fluoreszierende Protein dsRed trägt). Unter Bedingung 2 wurden überwiegend Synzytien gebildet, während diese unter Bedingung 1 trotz einer effizienten Infektion weitgehend fehlten.
Das humane Respiratorische Synzytial-Virus (RSV) ist eine der Hauptursachen für Infektionen der unteren Atemwege bei Kleinkindern und älteren Menschen, doch seine Pathogenese ist aufgrund der bislang unzureichenden Erforschung der viralen Pathogenese nach wie vor kaum verstanden. Lifeng Liu aus dem Team hat kürzlich in Zellkulturstudien gezeigt, dass die durch RSV induzierte Synzytiumbildung nicht nur zur viralen Zytopathogenese beiträgt, sondern auch die Virusausbreitung über bisher unbekannte Wege fördert. Er hat ein einzigartiges experimentelles System (Abb. 1) etabliert, um die diesem Prozess zugrunde liegenden Mechanismen zu untersuchen und dessen physiologische Relevanz zu verstehen.
Mit großzügiger Unterstützung durch das MUI-START-Programm für Nachwuchswissenschaftler wollen wir diese Ergebnisse sowohl in Zellkulturen als auch in klinisch relevanten 3D-Modellen der Atemwege validieren. Damit wollen wir die molekularen Mechanismen der Synzytiumbildung und der RSV-Ausbreitung im menschlichen Atemwegsepithel aufklären.
Kollaborationspartner:
Assoc.-Prof. PD Mag. Dr. Wilfried Posch, Abteilungsleiter. Professor für neu auftretende Infektionskrankheiten. Abteilung für Hygiene, Mikrobiologie und Virologie. Medizinische Universität Innsbruck.
Mag. Pharm. Stefanie Dichtl-Zweimüller, PhD, Klinik für Hals-Nasen-Ohren-Heilkunde und Kopf-Hals-Chirurgie, Medizinische Universität Innsbruck.
Hochmotivierte Studierende, die auf der Suche nach einem Betreuer für ihre Bachelor- oder Masterarbeit im Bereich Virologie sind, werden gebeten, sich für weitere Informationen an uns zu wenden.
Projekte
Verständnis grundlegender Mechanismen, die die Verformbarkeit von Insektenzellmembranen steuern
Dauer:
Oktober 2023 – September 2026
Details:
Insektenzellmembranen unterscheiden sich von Säugetiermembranen durch ihre Verformbarkeit, ihren Lipidgehalt und ihre Verteilung. Umhüllte Viren, die von Insekten übertragen werden, benötigen enge Interaktionen mit Zellmembranen, um in Zellen einzudringen, ihre Genome in Zellen zu replizieren und Zellen zu verlassen. Trotz grundlegender biophysikalischer Unterschiede zwischen Insekten- und Säugetiermembranen können Viren effektiv Zellen aus beiden Phyla infizieren. In jahrzehntelangen Studien über Insektenviren wurde der Mechanismus der Deformation von Insektenmembranen und ihre Ausnutzung durch Viren nicht untersucht. Unser neu gebildetes Team arbeitet an der Schnittstelle zwischen Insektengenetik, Biophysik und Infektionsbiologie und hat innovative Technologien zusammengestellt, um diese Barriere zu durchbrechen. Durch das kombinierte Fachwissen der PIs werden wir: 1. Gen-Editing-Bibliotheken in Insektenzellen verwenden, um Wirtsfaktoren zu identifizieren, die die Interaktionen zwischen Viren und Membranen steuern; 2. die Deformation von Membranen mit hoher Auflösung sichtbar machen; 3. die Auswirkungen der Deformation von Membranen auf die Durchlässigkeit für Viren, die von Insekten übertragen werden, bewerten. Diese Studien werden einen Einblick in die Mechanismen geben, die die Form der Insektenmembranen steuern, und unser Verständnis der Virusanpassung bei grundlegend verschiedenen Arten revolutionieren.
Drittmittel:
The International Human Frontier Science Program Organization (HFSP), 1.106.000 EUR
Die Rolle von Tetraspaninen bei der artenübergreifenden Übertragung von neu auftretenden Alphaviren
Dauer:
April 2022 – März 2025
Details:
Tetraspanine sind evolutionär konservierte integrale Membranproteine mit einer Länge von 200-350 Aminosäuren. Durch ihre große extrazelluläre Schleife vermitteln sie Protein-Protein- und Protein-Lipid-Interaktionen in Zellmembranen und bilden Membranmikrodomänen, die als „Tetraspanin-Netzwerke“ bekannt sind. Bei Menschen und Mäusen sind 33 Tetraspanine beschrieben worden, und Moskitoarten exprimieren mindestens 15 Tetraspanin-Orthologe. In Säugetierzellen sind Tetraspanine Wirtskofaktoren für verschiedene Viren, darunter Papillomviren, Influenzaviren, Hepatitis-C-Viren, HIV-1 und Coronaviren (Gerold et al, 2015; Bruening et al, 2018; Banse et al, 2018; Alberione et al, 2020; Palor et al, 2020). Für das Hepatitis-C-Virus haben Kollegen und wir gezeigt, dass das Tetraspanin CD81 ein Faktor ist, der den Wirtsbereich bestimmt (Vogt et al. 2013; Scull et al., 2015; von Schaewen et al., 2016).
Das vorgeschlagene Projekt zielt darauf ab, im Detail zu charakterisieren, welche der 33 menschlichen Tetraspanine neben CD81 Wirtsfaktoren für Alphaviren sind und ob Tetraspanine von Reservoir-Spezies, Dead-End-Wirtsspezies und übertragenden Moskito-Vektoren als Wirtsfaktoren von Alphaviren dienen. Die Arbeit wird somit zum Verständnis der molekularen Zusammensetzung und Funktion von Alphavirus-Replikationskomplexen beitragen und die Rolle der Tetraspanine für das Artenspektrum, die Übertragung und folglich die Entstehung von Alphaviren bestimmen.
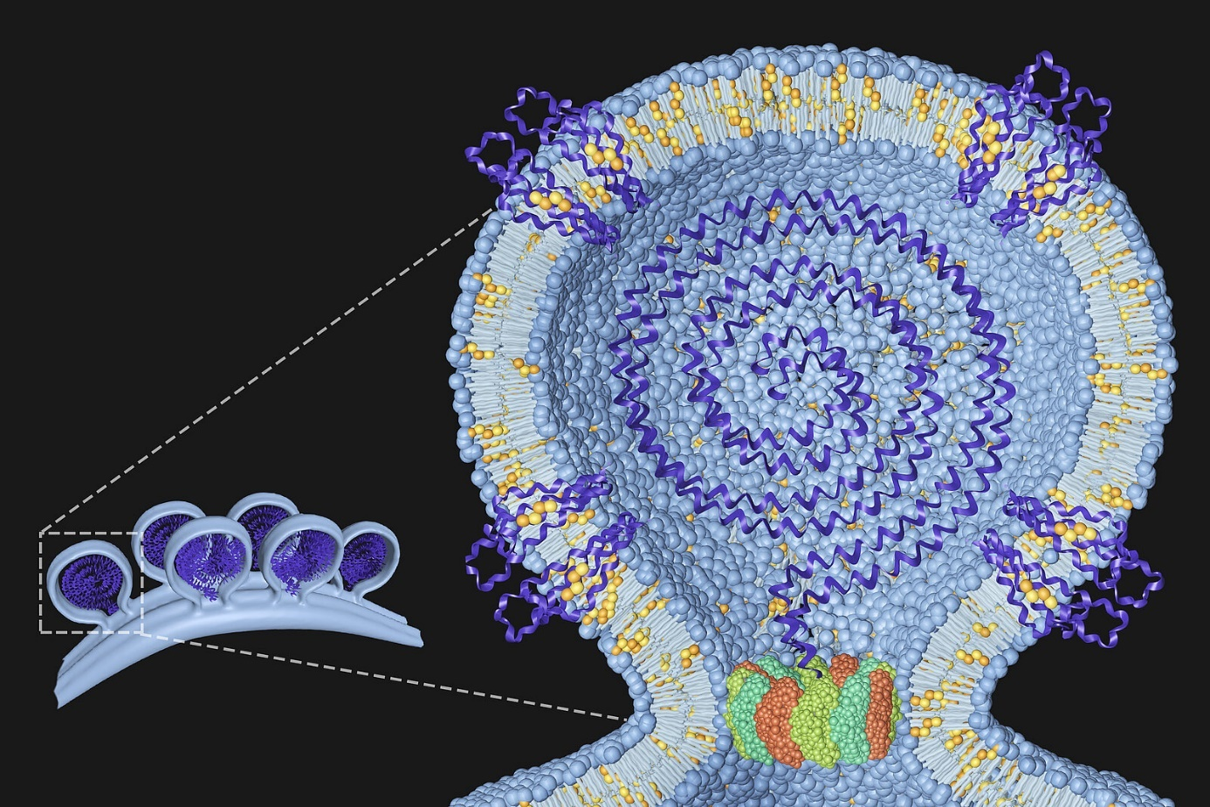
Unsere Gruppe ist daran interessiert, die Protein- und Lipiddeterminanten von Virusinfektionen zu verstehen. Die Abbildung zeigt ein Modell des Replikationskomplexes des Chikungunya-Virus an der Plasmamembran mit dem viralen Genom in der Mitte und Wirtsproteinen und Lipiden, die wir in der Membran eingebettet haben. Der dodekamere Ring am Hals repräsentiert das nicht-strukturelle Protein 1 (nsP1) des Chikungunya-Virus. Einzelheiten sind zu finden in Lasswitz et al., mBio 2022.
Drittmittel:
Deutsche Forschungsgesellschaft (DFG), 110.700 EUR
Entwicklung eines Ex-vivo-Modells zur Untersuchung der zoonotischen Übertragung von Noroviren
Dauer:
Mai 2023 – Oktober 2026
Details:
Noroviren sind die häufigste virale Ursache von akuter Gastroenteritis. Es sind mindestens 40 Noroviren bereits beschrieben worden, und es erscheinen regelmäßig neue Varianten. Die Entwicklung, Entstehung und Ausbreitung von Noroviren ist noch nicht vollständig geklärt. Insbesondere die Rolle eines potenziellen Reservoirs in Tieren ist noch nicht vollständig untersucht. Es gibt mehrere Hinweise auf die Übertragung von Noroviren zwischen Mensch und Tier. Bislang gibt es jedoch kein In-vitro-System, mit dem die Übertragung zwischen verschiedenen Arten untersucht werden kann. In diesem Projekt wollen wir ein Ex-vivo-System entwickeln, das auf Darmbiopsien von verschiedenen Tierarten basiert, um die Norovirus-Übertragung zwischen verschiedenen Arten experimentell zu untersuchen. Wir werden Biopsien von Hunden, Schweinen und Hühnern verwenden, da diese in großer Zahl vorkommen und in engem Kontakt mit Menschen stehen. Das Risiko einer Übertragung ist daher erhöht. Es werden Präzisions-Darmschnitte angefertigt und verwendet, um die Bindung, Invasion/Internalisierung und Replikation des Norovirus in den jeweiligen Wirtsgeweben zu untersuchen. Darüber hinaus soll die Rolle bekannter Empfänglichkeitsfaktoren, der Histo-Blutgruppenantigene, untersucht werden. Sobald dieses Explantatsystem etabliert ist, wird es die Untersuchung von Norovirus-Rezeptoren, Attachment-Faktoren und anderen Wirtsfaktoren bei Menschen und nicht-menschlichen Tierarten ermöglichen. Das System wird auch für die Untersuchung anderer Darmviren mit zoonotischem Potenzial nützlich sein, darunter Coronaviren, Influenzaviren und Noroviren von Hunden und Schweinen.
Drittmittel:
BMBF, 198.361 EUR
Modell für Arbovirus-Infektion der Haut - MOZART
Dauer:
Oktober 2023 – Juli 2025
Details:
Jedes Jahr sterben etwa 750.000 Menschen an durch Mücken übertragenen Krankheiten wie Malaria, Dengue-Fieber, Rifttalfieber und Chikungunya-Fieber. Es wird erwartet, dass die Häufigkeit dieser Krankheiten in den kommenden Jahrzehnten erheblich zunehmen wird, da sich die Verbreitungsgebiete mehrerer Moskitoarten aufgrund des Klimawandels ausweiten.
Stechmücken übertragen nicht nur Krankheiten, sondern können auch den Schweregrad der von ihnen übertragenen Krankheiten beeinflussen. Experimentelle Infektionen von Tieren haben gezeigt, dass die Übertragung von Arboviren durch Mückenstiche im Vergleich zu einer künstlichen Infektion zu einem Anstieg des Schweregrads der Krankheit führen kann. Es ist auch bekannt, dass der Speichel von Insekten und Zecken das Fortschreiten von durch Vektoren übertragenen Krankheiten fördern kann. Die Haut ist das erste Organ, das einer Arbovirusinfektion ausgesetzt ist, so dass die ersten Infektionsereignisse auch den Krankheitsverlauf maßgeblich bestimmen. Daher ist es für viele Forschungsfragen unerlässlich, eine natürliche Infektion der Haut durch einen Mückenstich zu untersuchen.
Bislang konnte dies nur durch in-vivo-Experimente (Tierversuche) erreicht werden. Das Ziel dieses Projekts ist es, eine Alternative zu entwickeln, indem aus ethischen und physiologischen Gründen Tiermodelle durch menschliche Hautexplantate ersetzt werden. Die Herausforderung dieser Studie besteht darin, einen Test zu etablieren, bei dem die Stechmücken die Hautexplantate als potenzielle Wirte erkennen. Ziel ist es, dass die Stechmücken die Hautexplantate erfolgreich stechen. In einem zweiten Schritt sollen beispielsweise mit dem Rifttalfieber-Virus (RVFV) und/oder dem Chikungunya-Virus (CHIKV) infizierte Stechmücken die Hautexplantate durch einen Stich infizieren. Im Erfolgsfall werden die Projektergebnisse eine Auswahl aus verschiedenen Modellen für zukünftige Forschungsfragen ermöglichen.
Drittmittel:
BMBF, 122.004 EUR
Identifizierung und Charakterisierung von Alphavirus-Wirtsfaktoren, die den Gewebetropismus beim Menschen bestimmen
Dauer:
Januar 2022 – Dezember 2025
Details:
Neue und wieder auftauchende Viren stellen ein ernstes Gesundheitsproblem dar. Insbesondere durch Stechmücken übertragene Infektionskrankheiten sind auf dem Vormarsch, da bestimmte Stechmückenarten in neue geografische Regionen vordringen. Alpha-Viren wie das Chikungunya-Virus (CHIKV) und das Venezolanische Pferdeenzephalitis-Virus (VEEV) gehören zu der Gruppe der durch Mücken übertragenen Viren. CHIKV verursacht lang anhaltende Arthritissymptome, während VEEV eine Hirnhautentzündung hervorruft. Warum die beiden eng verwandten Viren Krankheitssymptome in unterschiedlichen Geweben, d. h. in den Gelenken und nicht im zentralen Nervensystem, hervorrufen, ist weitgehend unbekannt. Diese Wissenslücke spiegelt sich in einem unzureichenden Verständnis der Wirtsfaktoren von CHIKV und VEEV wider. In diesem Forschungsprojekt bauen wir auf unseren Erkenntnissen auf, dass der Phosphatidylserin (PS)-Rezeptor TIM-1 (T-Zell-Immunglobulin-Mucin-Rezeptor) und ein Tetraspanin Wirtsfaktoren von CHIKV sind. Wir stellen die Hypothese auf, dass (a) VEEV ebenfalls PS-Rezeptoren und Tetraspanine als Wirtsfaktoren nutzt, (b) TIM-1 und das Tetraspanin mit anderen Proteinen interagieren, die die Infektion fördern, und (c) dass einige dieser Proteine zum Gewebetropismus von CHIKV und VEEV beitragen. Um unsere Hypothese zu überprüfen, werden wir zunächst modernste quantitative Proteomics-Techniken anwenden, um Eintrittsfaktoren und Rezeptoren von CHIKV und VEEV zu identifizieren. Anschließend werden wir die Rolle der PS-Rezeptoren und der 33 menschlichen Tetraspanine bei der VEEV-Infektion mithilfe der RNA-Interferenz testen. TIM-1 und Tetraspanin-assoziierte Proteine werden durch Proximity Labelling, hochauflösende Affinitätsanreicherung und Massenspektrometrie bestimmt. Schließlich werden wir den Beitrag der identifizierten Wirtsfaktoren zum Gewebetropismus von CHIKV und VEEV durch proteomische Analysen, Einzelzellsequenzierung und virologische Methoden analysieren. Insbesondere werden Hautorganoide infiziert und die viralen Zielzellen in der Haut sowie die Expression von Wirtsfaktoren bestimmt. Darüber hinaus werden wir Expressionsdaten aus Datenbanken und Gesamtzellproteom-Messungen von Fibroblasten und neuronalen Zellen in den Datensatz integrieren. Mit Hilfe modernster bioinformatischer Analysen (Feature Selection) werden wir dann Wirtsfaktoren bestimmen, die mit hoher Wahrscheinlichkeit zum Gewebetropismus und den unterschiedlichen Krankheitsbildern beitragen. Diese Wirtsfaktoren werden systematisch in relevanten menschlichen Zellen und schließlich in Mäusen ausgeschaltet, um ihren Beitrag zum Krankheitsbild in vitro und in vivo zu klären. Zusammenfassend lässt sich sagen, dass dieses Forschungsprogramm darauf abzielt, mechanistische Einblicke in den Infektionsprozess von zwei wichtigen humanen Krankheitserregern zu gewinnen. Die Ergebnisse werden zu einem besseren Verständnis der von CHIKV und VEEV verursachten Symptome führen und können Ansatzpunkte für Therapien zur Linderung oder Heilung von Chikungunya-Fieber und venezolanischer Enzephalitis liefern.
Drittmittel:
Deutsche Forschungsgesellschaft (DFG), 398.333 EUR
Verständnis der Rolle von Phosphatidylserinen und ihren Rezeptoren bei der artenübergreifenden Übertragung von Alphaviren
Dauer:
Oktober 2021 – Juni 2025
Details:
Alphaviren (Familie Togaviridae) sind neu auftretende und wieder auftauchende kleine umhüllte RNA-Viren, die von tierischen Reservoiren durch Stechmücken auf den Menschen übertragen werden und lähmende Gelenkschmerzen oder Enzephalitis verursachen können. Je nach Art des Reservoirs und des übertragenden Moskito-Vektors sind sie in verschiedenen geografischen Regionen zu finden. Während das Chikungunya-Virus (CHIKV) und das O’nyong’nyong-Virus (ONNV) historisch auf tropische und subtropische Klimazonen beschränkt waren, sind das Sindbis-Virus (SINV) und das Ross-River-Virus (RRV) hauptsächlich in Skandinavien bzw. Australien zu finden. Die Anpassung des CHIKV an neue Moskito-Vektoren und die globale Erwärmung haben zum Auftreten des Virus in Europa geführt und es zu einem potenziellen Problem für die öffentliche Gesundheit in Deutschland und den Nachbarländern gemacht. Eine Einschleppung des venezolanischen
Pferdeenzephalitis-Virus (VEEV), das auf dem amerikanischen Kontinent zirkuliert und neurologische Symptome bei Pferden und Menschen verursacht, ist ebenfalls möglich. Bislang gibt es keine Humanimpfstoffe oder antiviralen Medikamente gegen arthritogene und neurotrope Alphaviren auf dem Markt. Dies ist darauf zurückzuführen, dass die molekularen Mechanismen des Infektionsprozesses und die kritischen Wirtsfaktoren, die an der Infektion mit Alphaviren und der artübergreifenden Übertragung beteiligt sind, nicht bekannt sind. Kürzlich fand unser Team heraus, dass der Phosphatidylserin-Rezeptor T-Zell-Immunglobulin und Mucin-Domäne 1 (TIM-1) ein CHIKV-Anheftungsfaktor ist. Eine weitere prominente Gruppe von Phosphatidylserin-Rezeptoren ist die Tyro3-, AXL- und MerTK (TAM)-Rezeptor-Tyrosinkinase (RTK)-Familie, die die drei Proteine Tyro3, AXL und MerTK umfasst. Die physiologische Funktion der TIM- und TAM-Rezeptoren besteht darin, apoptotische Körper zu binden und zu internalisieren, die Phosphatidylserin auf dem äußeren Membranblatt freisetzen. Wir konnten zeigen, dass TIM-1, aber nicht AXL, als Wirtsfaktor für CHIKV dient. Darüber hinaus ist die Phosphatidylserin-Bindungsdomäne von TIM-1, die so genannte Metallionen-Liganden-Bindungsstelle (MILIBS), entscheidend für die Wirtsfaktor-Funktion von TIM-1 im Zusammenhang mit der CHIKV-Infektion. TIM-1 beeinflusst sowohl die Bindung als auch die Internalisierung von CHIKV-Partikeln in menschlichen Zellen. Schließlich verstärkt TIM-1 auch die CHIKV-Infektion in Keratinozyten, die zu den ersten Zielzellen des Virus nach einem Mückenstich gehören. Wir stellen daher die Hypothese auf, dass Alphaviren, einschließlich CHIKV, Phosphatidylserin-Rezeptoren für die Zellanlagerung und den Eintritt in Reservoir-Spezies wie nicht-menschliche Primaten und in übertragende Moskito-Vektoren nutzen. Darüber hinaus wollen wir klären, ob das in Insektenzellen produzierte Virus auch Phosphatidylserin freisetzt und ob dies bei der Infektion menschlicher Zellen, also bei der artenübergreifenden Übertragung, hilfreich ist. Und schließlich wollen wir klären, wie Phosphatidylserin auf der Virushülle exponiert wird.
Diese Arbeiten werden zum Verständnis der molekularen Zusammensetzung von Alphavirus-Partikeln, der Funktion von Alphavirus-Anheftungsfaktoren und der Rolle der apoptotischen Mimikry bei der speziesübergreifenden Übertragung und folglich der Entstehung von Alphaviren beitragen.
Drittmittel:
Deutscher Akademischer Austauschdienst (DAAD), 48.000 EUR




